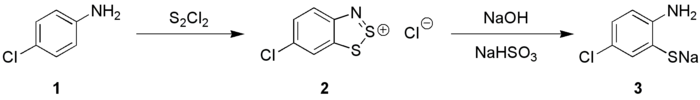
Реакция Херца — метод синтеза 2-аминотиофенолов из ароматических аминов взаимодействием дитиодихлорида с анилинами (1), ведущим к образованию циклических 1,2,3-бензодитиазолиевых солей (2, соли Херца) и последующим расщеплением дитиазолиевого цикла:
Варианты и модификации
В реакцию вступают различные ароматические и гетероароматические амины, а также их N-ацилпроизводные (N-ацетил-2-нафтиламин[1], 3- и 4-аминоизохинолины[2].
Сам анилин в условиях реакции Херца подвергается хлорированию в пара-положение по отношению к аминогруппе[3], p-замещенные анилины в условиях реакции Херца хлорированию не подвергаются.
В зависимости от условий гидролиза солей Херца могут быть получены различные продукты.
Так, при действии азотистой кислоты на солей Херца происходит перегруппировка в 1,2,3-бензотиадиазолы, сопровождающаяся хлорированием ароматического кольца, реакция проходит через размыкание 1,2,3-бензодитиазолиевого цикла с последующим диазотированием аминогруппы и электрофильное внутримолекулярное присоединение диазониевой группы к тиольной[4]:
однако основным методом гидролиза солей Херца является под действие едкого натра или бисульфита натрия в сильнощелочной, в результате чего образуются 2-аминотиофеноляты:
Синтетическое применение 2-аминотиофенолов
2-Аминотиоляты и 2-аминотиофенолы широко используются в синтезе гетероциклических соединений — их ацилирование является препаративным методом синтеза бензотиазолов:
Алкилирование хлоруксусной кислотой 2-аминотиофенолятов, полученных в реакции Херца, с образованием 2-аминоарилтиогликолевой кислоты (6) и дальнейшая замена в ней аминогруппы на нитрильную по Зандмейеру с последующим омылением и циклизацией является одним из промышленных методов синтеза тиоиндоксилов (7) — важных полупродуктов в синтезе тиоиндигоидных красителей (8, 9)[5]:
Примечания
- ↑ Katritzky, Alan R.; Steven V. Ley, Otto Meth-Cohn, Charles Wayne Rees. Comprehensive Organic Functional Group Transformations: Synthesis: carbon with one heteroatom attached by a single bond (англ.). — Elsevier, 1995. — P. 708. — ISBN 9780080423234.
- ↑ Weissberger, Edward C. Taylor, Peter Wipf, Arnold. Chemistry of heterocyclic compounds (неопр.). — John Wiley and Sons, 2004. — С. 168. — ISBN 9780471326625.
- ↑ Huestis, Laurence D.; Marilyn L. Walsh, Nancy Hahn. The Herz Reaction. The Formation and Hydrolysis of Herz Compounds (англ.) // J. Org. Chem.[англ.] : journal. — 1965. — Vol. 30, no. 8. — P. 2763—2766. — ISSN 0022-3263. — doi:10.1021/jo01019a061.
- ↑ Ellis, Gwynn Pennant. Synthesis of fused heterocycles (неопр.). — John Wiley & Sons, 1992. — С. 986. — ISBN 9780471930709.
- ↑ Zollinger, Heinrich. Color chemistry: syntheses, properties, and applications of organic dyes and pigments (англ.). — Helvetica Chimica Acta, 2003. — P. 255—256. — ISBN 9783906390239.
Обычно почти сразу, изредка в течении часа.