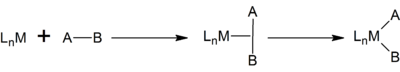Окислительное присоединение — это один из типов реакций, встречающихся в металлорганической химии.[1][2][3][4] Оно заключается в присоединение органического субстрата к атому металла с одновременным увеличением его формальной степени окисления на +2. Окислительное присоединение часто является частью каталитических циклов наряду с обратной реакцией восстановительного элиминирования.[5]
В химии переходных металлов
Для протекания окислительного присоединения необходимо, чтобы центральный атом металла мог существовать в двух устойчивых степенях окисления n и n+2 [6]. Типичные примеры таких пар: Ru0/Ru+2, Rh+1/Rh+3, Pd0/Pd+2. Окислительное присоединение менее характерно для 3d металлов, которые имеют устойчивые степени окисления, отличающиеся только на единицу, например, Fe+2/Fe+3, Co+2/Co+3.[5]
На скорость окислительного присоединения влияет несколько факторов:[5]
- Присоединение протекает быстрее в комплексах металлов, которые богаты электронами и находятся в низких степенях окисления. Например, комплекс Ni0(PEt3)4 реагирует с арилгалогенидами, а комплекс с акцепторными лигандами Ni0(PF3)4 или Ni + 2 Cl2(PEt3)2 – нет.
- Присоединение протекает быстрее в комплексах, где металл пространственно более доступен. Металлы первого переходного ряда менее охотно вступают в окислительное присоединение отчасти потому, что образуют более короткие связи с лигандами и, следовательно, более экранированы.
- Большое влияние на скорость и саму возможность окислительного присоединения оказывает прочность исходной связи в реагенте X−Y и прочность образующихся связей M−X и M−Y. Например, среди арилгалогенидов наибольшую активность в реакциях окислительного присоединения к палладию (а значит и в каталитических реакциях С−С сочетания) проявляют иодиды, а не более полярные арилхлориды: связь С−I слабее, чем C−Cl, а образующаяся связь Pd−I более прочная, чем Pd−Cl в соответствии с принципом жесткости-мягкости по Пирсону.
Механизмы окислительного присоединения
Механизм окислительного присоединения зависит от металла и субстратов.
Согласованный механизм
По этому механизму происходит окислительное присоединение неполярных субстратов, таких как водород или углеводороды. В таких субстратах отсутствует π-связь, поэтому образуется трехцентровый σ-комплекс с последующим разрывом внутримолекулярной связи лиганда (вероятно, за счет перехода электронной пары на σ-орбиталь межлигандной связи) с образованием окисленного комплекса. Обычно происходит цис-присоединение, хотя в дальнейшем продукт может изомеризоваться в транс-комплекс. Обратное восстановительное элиминирование протекает только при цис-расположении уходящих групп.[5]
Этот механизм применим к образованию гомоядерной молекулы, например, H2. Многие реакции активации C–H-связи также идут по согласованному механизму посредством образования связей M–(C–H).[2]
Типичным примером является реакция водорода с комплексом Васка, транс-IrCl(CO)[P(C6H5)3]2. В этом случае иридий меняет свою формальную степень окисления с +1 на +3. Продукт формально связан с тремя анионами: одним хлоридным и двумя гидридными лигандами. Как показано ниже, исходное соединение представляет собой 16-электронный четырехкоординационный комплекс, а продукт - шестикоординационный 18-электронный комплекс.
SN2-механизм
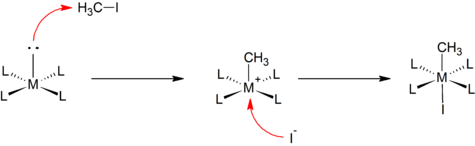
Окислительное присоединение может протекать аналогично реакциям бимолекулярного нуклеофильного замещения в органической химии. Металлический центр нуклеофильно атакует менее электроотрицательный атом в субстрате, что приводит к разрыву связи R–X с образованием соединения [M–R]+. Затем происходит быстрая координация аниона с катионом на металле. Примером может служить реакция плоско-квадратного комплекса с метилиодидом:
SN2-механизм предполагается в случае полярных и электрофильных субстратов, таких как алкилгалогениды и галогены.[2]
Ионный механизм
Ионный механизм подобен SN2-механизму, т.к. в нем тоже происходит ступенчатое присоединение двух отдельных фрагментов лиганда. Ключевым отличием является то, что по ионному механизму реагируют субстраты, диссоциирующие в растворе до взаимодействия с металлическим центром. Примером ионного окислительного присоединения является присоединение соляной кислоты.
Радикальный механизм
Алкилгалогениды и подобные субстраты могут присоединяться к металлическому центру не только по SN2-механизму, но также и по радикальному механизму. В настоящее время некоторые аспекты механизма все еще обсуждаются, однако существуют примеры реакций, которые идут по радикальному механизму:[7]
- Инициирование цепи
- [(CH3)2C(CN)N]2 → 2 (CH3)2(CN)C• + N2
- (CH3)2(CN)C• + PhBr → (CH3)2(CN)CBr + Ph•
- Развитие цепи
- Ph• + [Pt(PPh3)2] → [Pt(PPh3)2Ph]•
- [Pt(PPh3)2Ph]• + PhBr → [Pt(PPh3)2PhBr] + Ph•
Применения
Окислительное присоединение (и обратная ей реакция восстановительного элиминирования) являются ключевыми стадиями в большинстве каталитических циклов, например, в реакциях Сузуки, Соногаширы и др. Например, в реакции кросс-сочетания Кумады за счет окислительного присоединения активируется исходный субстрат арилбромид, а за счет восстановительного элиминирования регенерируется активная частица L2Ni0 и образуется органический продукт. Движущей силой последнего процесса является формирование прочной связи C–C из относительно слабых связей Ni–C.[5]
Примечания
- ↑ Jay A. Labinger "Tutorial on Oxidative Addition" Organometallics, 2015, volume 34, pp 4784–4795. doi:10.1021/acs.organomet.5b00565
- ↑ 1 2 3 Crabtree, Robert. The Organometallic Chemistry of the Transition Metals. — Wiley-Interscience, 2005. — P. 159–180. — ISBN 0-471-66256-9.
- ↑ Miessler, Gary L. Inorganic Chemistry / Gary L. Miessler, Donald A. Tarr. — 3rd.[ISBN?]
- ↑ Shriver, D. F. Inorganic Chemistry / D. F. Shriver, P. W. Atkins.[ISBN?]
- ↑ 1 2 3 4 5 Перекалин Д.С. Металлоорганическая химия и немного катализа. — М. : Перо, 2019. — 80 с. — ISBN 978-5-00150-431-3.
- ↑ IUPAC Gold Book internet edition: «oxidative addition».
- ↑ Hall, Thomas L.; Lappert, Michael F.; Lednor, Peter W. (1980). “Mechanistic studies of some oxidative-addition reactions: free-radical pathways in the Pt0-RX, Pt0-PhBr, and PtII-R′SO2X Reactions (R = alkyl, R′ = aryl, X = halide) and in the related rhodium(I) or iridium(I) Systems”. J. Chem. Soc., Dalton Trans. (8): 1448—1456. DOI:10.1039/DT9800001448.
Обычно почти сразу, изредка в течении часа.