Макроэргические молекулы (макроэрги) — биологические молекулы, которые способны накапливать и передавать энергию в ходе реакции. При гидролизе одной из связей высвобождается более 20 кДж/моль. По химическому строению макроэрги — чаще всего ангидриды фосфорной и карбоновых кислот (см. Ангидриды карбоновых кислот), а также слабых кислот, какими являются тиолы и енолы.
Энциклопедичный YouTube
-
1/3Просмотров:101 8283 0881 210
-
АТФ: Аденозинтрифосфат(видео 10) | Энергия | Биология
-
Шноль С. Э. - Введение в биоорганическую химию - Макроэргические молекулы, цикл Кребса
-
Гладилин А. К. - Биохимия - Высокоэнергетические соединения
Субтитры
АТФ — одна из самых важных биологических молекул. Это аденозинтрифосфат. Аденозинтрифосфат. Сложное слово... да, странное название. Но такое встречается в биологии. Однако всё, что вам нужно знать то, что присутствие АТФ в биохимической реакции означает использование в ней биологической энергии. Ещё его можно считать разменной монетой в процессах энергообеспечения. Итак, я повторю: можно считать его разменной монетой в процессах энергообеспечения. Что же всё это значит? Важна энергия связей АТФ. Сейчас объясню. Пока вы ещё не знаете, как выглядят аденозин и фосфат, поэтому я изображу молекулу АТФ схематически. Это, к примеру, будет аденозин. Вот так. С ним связано три остатка фосфорной кислоты. Вот так они присоединяются. Это АТФ. Аденозинтрифосфат. Потому что 3 остатка фосфорной кислоты. Связи в молекуле аденозинтрифосфата способны гидролизоваться в присутствии воды. Нарисую воду. Молекула H2O. Одна из фосфатных групп отщепляется. Молекула воды разделяется между фосфатными группами — отщепившейся и оставшейся. Я расскажу об этом подробнее, но сперва в общих чертах. Остался аденозин с двумя фосфатными группами. Это аденозиндифосфат — АДФ. АДФ У трифосфата 3 фосфатных группы, а у дифосфата их осталось две Итак, дифосфат - это две фосфатные группы. При гидролизе АТФ отщепляется одна из фосфатных групп. Получается АДФ и свободная фосфорная кислота. Но самое главное — выделяется энергия. Выделяется энергия. Вот почему это разменная монета энергообеспечения, как я сказал выше. При наличии АТФ нужно всего лишь химически отщепить фосфатную группу, чтобы получить энергию. Её можно превратить в тепло или энергию для энергозависимых реакций, чтобы эти реакции могли происходить. Я изобразил молекулы в виде кружков, но точность нам не нужна. Вам нужно понять функциональную роль АТФ в биологических системах. Можно и запасать энергию в виде АТФ. Для этого нужно повернуть реакцию вспять. Таким образом энергия запасается. В этой части уравнения запас энергии, а в этой — использование энергии. Теперь вы на 95% знаете функции АТФ в биологических системах. Это запас энергии в связях. Энергия выделяется при отщеплении фосфата. Энергия запасается при синтезе аденозинтрифосфата. АТФ — это батарейка. Эта молекула накапливает энергию. Я изобразил аденозин кружком. Но не помешает знать, как он на самом деле выглядит Это картинка из Википедии. Я начал не с неё, потому что так было проще. Идея использования АТФ как энергоносителя довольно проста. Одна из трёх фосфатных групп отщепляется, выделяющаяся энергия поступает в систему. Чтобы присоединить фосфат, нужна энергия. Такова основная идея. А вот формула АТФ. И эта формула не настолько уж сложна. Возьмём аденозин. Молекулу аденозина. Где же он? Вот аденозин. Вот эта часть молекулы. Это и есть аденозин. Если вы внимательно смотрели другие ролики, то узнали эту часть аденозина. Вот эта часть молекулы — аденин. Итак, эта часть молекулы является аденином. Тот самый нуклеотид, что входит в состав молекулы ДНК. В биологических системах молекулы используются по-разному. Это тот же аденин, о котором мы говорили. Это пуриновое основание, то же самое. Та же молекула. Интересный факт: молекула, входящая в состав ДНК, также участвует в энергообеспечении. Итак, в состав аденозина входит аденин. Он соединяется с рибозой. Рибоза также входит в состав РНК. Повторю: рибоза входит в состав РНК. И там, и здесь участвует рибоза. Однако сейчас разговор не об этом. Это пятиатомный сахар. Здесь не подписано, но подразумевается, что это углерод. Вот один атом, вот 2, 3, 4 и 5 атомов углерода. И это хорошо, что здесь используются элементы ДНК. Знакомые нам молекулы, которые встречаются постоянно. Но знания или зазубривания формулы не требуется, чтобы понять роль АТФ в биологических реакциях. А вот 3 фосфатные группы, их молекулярные формулы. Льюисовские формулы. Вот одна, вот вторая фосфатная группа, и вот третья. Вот они все. Когда я изучал это, у меня возникли вопросы. Я могу поверить, что если гидролизовать одну из этих связей, то выделится энергия. Но мне никто не отвечал на главный вопрос. Почему? Что в этой связи такого особенного? Любая связь — это общая электронная пара двух атомов. Давайте рассмотрим подробнее. Эта связь представлена общими электронами, общими электронами атомов фосфатных групп. Из периодической таблицы вы знаете, что у фосфора 5 валентных электронов. Кислород более электроотрицателен и отнимает электрон. Но электрону очень неудобно. На то есть несколько причин. Электрон высокоэнергичен. Посмотрите на все эти отрицательные заряды. Они стремятся оттолкнуться друг от друга. Поэтому электроны связи находятся далеко от ядра. У них высокая энергия. Это, конечно, упрощение На самом деле всё куда сложнее. Это целый мир квантовой механики. Но мы упрощаем и считаем, что группы атомов отталкиваются друг от друга, а энергия электрона повышается. Электрон находится очень далеко от ядер атомов. И когда фосфатная группа отщепляется, энергия этих электронов снижается, а излишек выделяется. Любая энергия, выделяющаяся в любой химической реакции возникает за счёт снижения энергии электронов. Это необходимо зафиксировать письменно. Итак, любая энергия, выделяющаяся в любой химической реакции возникает за счёт снижения энергии электронов. Я обязательно расскажу о клеточном дыхании и гликолизе, там будет выделяться энергия. Всё это из-за снижения энергии электронов. Здесь можно провести аналогию. Если я, скажем, лечу на самолёте, у меня много потенциальной энергии и я чувствую себя некомфортно. А если я смотрю футбол на диване, потенциальной энергии мало и мне удобно. Плюхнувшись на диван я выделю энергию. Как-то так. Странные у меня аналогии, но тем не менее. Я хочу объяснить вам, как на самом деле происходит реакция. После этого ролика вы будете знать, что АТФ используется в 95% биологических процессов. Но как эта реакция выглядит на самом деле? Надо будет кое-что скопировать и затем вставить. Я уже говорил, что эта группа отщепляется от АТФ. Отщепляется фосфатная группа. Итак, давайте я скопирую и вставлю. Это отщепляемая фосфатная группа, а вот остаток. Остался АДФ. Вот АДФ. Не буду копировать целиком. Я ведь знаю, что это аденозин. Итак, копирую и вставляю. Отлично. Итак, связь гидролизовалась. При этом выделилась энергия. Но я хочу показать вам механизм. Схематически показать, как всё происходит. Реакция идёт в присутствии воды. Нарисую воду. Кислород и водород. И ещё один водород. Вот наша вода. В ходе реакции гидролиза этот атом должен с чем-то связаться, заполучив общую электронную пару. Пусть этот атом водорода присоединится сюда, разделив свои электроны с кислородом... с кислородом. А у атома фосфора остался не поделённый электрон. Атом фосфора может разделить пятый электрон с атомом кислорода. Его 4 электрона уже поделены. И если водород уходит вправо, остаётся эта группа OH, с которой фосфор может разделить электроны. Присоединяем OH. Вот что происходит на самом деле. Можно и по-другому. Расщепим здесь. Вот по этой связи. Здесь будет атом кислорода, присоединится водород. А здесь присоединится группа OH. Либо так, либо так. Всё равно. И есть ещё кое-что, но это уже сложнее. Я даже не хотел об этом говорить. Я сказал, что снижение энергии обусловлено тем, что после расщепления электрон перейдёт в более удобное для него самого состояние. Его энергия снизится, потому что ему не придётся находиться между группами атомов, которые взаимно отталкиваются по причине отрицательных зарядов. Это ещё не всё. Вторая причина требует отдельного объяснения в ходе изучения органической химии. Это резонанс. Это более резонансная структура. Это означает, что эти электроны смогут перемещаться между атомами, а это повышает устойчивость. И вот у этого атома кислорода есть лишний электрон. Этот лишний электрон может образовать двойную связь с атомом фосфора. Двойную связь с атомом фосфора. А этот электрон может переместиться сюда. С этой стороны и с другой. Не хочу вдаваться в подробности, но это повышает устойчивость. Если вы уже изучали органическую химию, то поймёте. Но не заостряйте на этом внимание. Самое важное — это то, что при отщеплении фосфатной группы выделяется энергия, расходуемая на всякие биологические функции, например рост и движение, работу мышц, генерацию электрических импульсов в нервах и в мозгу. Это главный энергоноситель в биологических системах. Вот что нужно знать об АТФ. Subtitles by the Amara.org community
Классификация макроэргов по связям
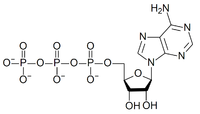
1. Фосфоангидридная связь. ΔG — 32 кДж/моль. Представители: все нуклеозидтрифосфаты и нуклеозиддифосфаты (АТФ, ГДФ и их аналоги)
2. Тиоэфирная связь. ΔG — 34 кДж/моль. Представители: ацетил-КоА, сукцинил-КоА.

3. Гуанидинфосфатная связь. ΔG — 42 кДж/моль. Представители: креатинфосфат.

4. Ацилфосфатная связь(ацил — остаток жирной кислоты). ΔG — 46 кДж/моль. Представители: 1,3-бисфосфоглицерат.

5. Енолфосфатная связь. ΔG — 54 кДж/моль. Представители: фосфоенолпируват.
Литература
- Ленинджер А. Основы биохимии. В 3 томах. — М.: Мир, 1985
- Макроэргические соединения — статья из Большой советской энциклопедии.
См. также
Обычно почти сразу, изредка в течении часа.
