Термин геометрическая координация используется в целом ряде смежных областей химии — химии/физики твердого тела и не только.
Молекулы
Координационная геометрия атома в геометрическом соединении, образованном атомами вокруг центрального атома.
Координационные комплексы неорганических соединений
В области неорганических геометрических комплексов координации эти соединения являются геометрическими моделями, образованными атомами лигандов, которые связаны с центральным атомом в молекуле и комплексным соединением. Геометрическое расположение варьируется в зависимости от количества и типа лигандов, связанных с центром, состоящим из металла, а также координационного преимущества (англ. the coordination preference) центрального атома, как правило, металла в координационном комплексе. Число соединений (то есть число σ-связей между центральным атомом и лигандами), называется координационным числом. Геометрическая модель может быть описана как многогранник, где вершины многогранника являются центрами координации атомов лигандов.
Координационное преимущество металла часто варьируется в зависимости от его степени окисления. Число координационных связей (координационное число) может варьироваться от двух до 20.
Одна из самых распространенных геометрических координаций — октаэдрическая, где шесть лигандов координируются к металлу симметричным распределением, что ведет к образованию октаэдра, если линии нарисованы между лигандами. Менее встречающиеся в общей геометрии координации являются формы тетраэдра и «плоского квадрата» (2D квадрат).
Теория кристаллического поля может быть использована для объяснения относительной устойчивости соединений переходных металлов различной геометрической координации, а также наличия или отсутствия парамагнетизма.
ТОЭП может быть использована для предсказания геометрии комплексов основных элементов группы (исключение составляют актиноиды и лантаноиды).
Кристаллографическое использование
В кристаллической структуре геометрическая модель атома является геометрической структурой координации атомов, где определение координации атомов зависит от связей в модели. Например, в каменной соли, ионный состав каждого атома натрия содержит шесть ближайших соседних хлорид-ионов в октаэдрической геометрии и каждый хлорид аналогично — шесть соседних ионов натрия в октаэдрической геометрии. В металлах с объемноцентрированной структурой каждый атом имеет связь с восмью ближайшими другими атомами с кубической геометрией. В металлах с гранецентрированной кубической структурой каждый атом имеет двенадцать связей с соседними атомами с кубооктаэдрической геометрией.
| Координационное число | Геометрия | Изображение | Примеры дискретных (конечных) комплексов | Примеры на кристаллах |
|---|---|---|---|---|
| 2 | линейная | Ag(CN)2− в KAg(CN)2 | Ag в цианиде серебра, Au в AuI | |
| 3 | плоский треугольник | 
|
Cu(CN)32− в Na2Cu(CN)3·3H2O | O в TiO2 (структура рутила) |
| 4 | тетраэдр | 
|
CoCl42− | Zn и S в сульфиде цинка, Si в диоксиде кремния |
| 4 | квадрат | 
|
AgF4− | CuO |
| 5 | тригональная бипирамидальная | 
|
SnCl5− | |
| 5 | квадратная пирамидальная | 
|
InCl52− в (NEt4)2InCl5 | |
| 6 | октаэдр | 
|
Fe(H2O)62+ | Na и Cl в хлориде натрия |
| 6 | тригональная призматическая | 
|
Mo(SCHCHS)3 | As в NiAs, Mo в MoS2 |
| 7 | пентагональная бипирамидальная | 
|
ZrF73− в (NH4)3ZrF7 | Pa в PaCl5 |
| 7 | гранецентрированная октаэдрическая | [HoIII(PhCOCHCOPh)3(H2O)] | La в La2O3 | |
| 7 | тригональная призматическая, квадратическая моногранецентрированная | TaF72− в K2TaF7 | ||
| 8 | куб | Хлорид цезия, фторид кальция | ||
| 8 | квадратная антипризматическая | 
|
TaF83− в Na3TaF8 | Хлорид тория(IV) |
| 8 | додекаэдр | 
|
Mo(CN)84− в K4[Mo(CN)8].2H2O | Zr в K2ZrF6 |
| 8 | гексагональная бипирамидальная | 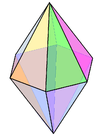
|
N в Li3N | |
| 8 | октаэдр | Ni в арсениде никеля | ||
| 8 | тригональная призматическая | Ca в CaFe2O4 | ||
| 8 | тригональная призматическая, квадратная лицевая двуребристая | PuBr3 | ||
| 9 | тригональная призматическая, квадратная лицевая триребристая | 
|
[ReH9]2− в нонагидроренате калия | SrCl2·6H2O , Th в RbTh3F13 |
| 9 | англ. monocapped square antiprismatic | [Th(торополонат)4(H2O)] | La в LaTe2 | |
| 10 | англ. bicapped square antiprismatic | Th(C2O4)42− | ||
| 11 | Th в [ThIV(NO3)4(H2O)3] (NO3−) | |||
| 12 | икосаэдр | 
|
Th в Th(NO3)62−-ион в Mg[Th(NO3)6]·8H2O | |
| 12 | кубооктаэдрон | 
|
ZrIV(η³−(BH4)4) | |
| 12 | антикубооктаэдон | 
|
||
| 14 | двуребристая антипризматичная гексагональная | U(BH4)4 |
Где нет дискретных комплексов означает, что соединения найдены как отдельные единицы сфер вокруг атомов в кристаллах
Именование неорганических соединений
ИЮПАК ввел полиэдрический символ (англ. Polyhedral symbol) в части «рекомендации номенклатуры по ИЮПАК в неорганической химии 2005» (англ. IUPAC nomenclature of inorganic chemistry 2005 recommendations) для описания геометрии вокруг атома в соединении.
IUCr (International Union of Crystallography) предложили символ, который показывается как верхний индекс в квадратных скобках в химической формуле. Например, CaF2 будет записан как Ca[8СВ]F2[4T], где [8СВ] означает что это кубическая координация и [4T] означает — четырехгранная. Эквивалентный символ в ИЮПАК обозначается как CU−8 и T-4 соответственно.
Символ ИЮПАК применим к комплексам и молекулам, в то время как по предложению IUCr это относится к кристаллическим твердым телам.
См. также
- Молекулярная геометрия
- Теория поля лигандов
Обычно почти сразу, изредка в течении часа.
